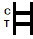Test rapide de la fibronectine fœtale
Utilisation détendue
Le fort®Le test du PROM est un test immunochromatographique visuellement interprété destiné à être utilisé pour la détection qualitative de la fibronectine fœtale dans les sécrétions cervicovaginales. La présence de fibronectine fœtale dans les sécrétions cervicovaginales entre 22 semaines, 0 jours et 34 semaines, 6 jours de gestation estassocié à un risque élevé d'accouchement prématuré.
Trodduction
La prestation prématurée, définie par l'American College of Obstetriciens and Gynecologists comme livraison avant la 37e semaine de gestation, est responsable de la majorité de la morbidité et de la mortalité périnatales non chromosomiques. Les symptômes de l'administration prématurée menacée comprennent les contractions utérines, le changement de débit vaginal, les saignements vaginaux, les maux de dos, l'inconfort abdominal, la pression pelvienne et les crampes. Les modalités de diagnostic pour l'identification de l'administration prématurée menacée comprennent la surveillance de l'activité utérine et les performances d'un examen cervical numérique, ce qui permet d'estimer les dimensions cervicales. Ces méthodes se sont révélées limitées, car une dilatation cervicale minimale (<3 centimètres) et une activité utérine se produisent normalement et ne sont pas nécessairement diagnostiques de l'administration prématurée imminente. Bien que plusieurs marqueurs biochimiques sériques aient été évalués, aucun n'a été largement accepté pour une utilisation clinique pratique.
La fibronectine fœtale (FFN), une isoforme de fibronectine, est une glycoprotéine adhésive complexe avec un poids moléculaire d'environ 500 000 daltons. Matsuura et ses collègues ont décrit un anticorps monoclonal appelé FDC-6, qui reconnaît spécifiquement III-CS, la région définissant l'isoforme fœtale de la fibronectine. Des études immunohistochimiques sur les placentae ont montré que le FFN estconfiné à la matrice extracellulaire de la région définissant la jonctiondes unités maternelles et fœtales de l'utérus.
La fibronectine fœtale peut être détectée dans les sécrétions cervicovaginales de femmes tout au long de la grossesse en utilisant un immunodosage monoclonal basé sur des anticorps. La fibronectine fœtale est élevée dans les sécrétions cervicovaginales au début de la grossesse, mais est diminuée de 22 à 35 semaines en grossesses normales. L'importance de sa présence dans le vagin au cours des premières semaines de grossesse n'est pas comprise. Cependant, il peut simplement refléter la croissance normale de la population de trophoblastes extravilleuses et du placenta. La détection de FFN dans les sécrétions cervicovaginales entre 22 semaines, 0 jours et 34 semaines, 6 jours, la gestation serait associée à l'administration prématurée dans les femmes symptomatiques et entre 22 semaines, 0 jours et 30 semaines, 6 jours chez les femmes enceintes asymptomatiques.
PRINCIPE
Le fort®Le test FFN utilise la technologie immunochromatographique de couleur et le flux capillaire. La procédure d'essai nécessite la solubilisation de FFN à partir d'un tampon vaginal en mélangeant l'écouvillon dans un tampon d'échantillon. Ensuite, le tampon d'échantillonnage mixte est ajouté à l'échantillon de cassette de test bien et le mélange migre le long de la surface de la membrane. Si FFN est présent dans l'échantillon, il formera un complexe avec l'anticorps anti-FFN primaire conjugué à des particules colorées. Le complexe sera alors lié par un deuxième anticorps anti-FFN enduit sur la membrane de nitrocellulose. L'apparition d'une ligne de test visible avec la ligne de contrôle indiquera un résultat positif.
Composants du kit
| 20 Individuellement packdispositifs de test ED | Chaque dispositif contient une bande avec des conjugués colorés et des réactifs réactifs précoés dans les régions correspondantes. |
| 2ExtractionFlacon de tampon | Saline tamponnée au phosphate 0,1 M (PBS) et 0,02% d'azide de sodium. |
| 1 écouvillon de contrôle positif (sur demande uniquement) | Contiennent du FFN et de l'azide de sodium. Pour le contrôle externe. |
| 1 écouvillon de contrôle négatif (sur demande uniquement) | Ne contient pas FFN. Pour le contrôle externe. |
| 20 Tubes d'extraction | Pour les spécimens de préparation à utiliser. |
| 1 Poste de travail | Place pour les flacons et tubes de tampon de maintien. |
| 1 Insert de package | Pour l'instruction de fonctionnement. |
Matériaux requis mais non fournis
| Minuteur | Pour une utilisation du timing. |
PRÉCAUTIONS
■ Pour une utilisation diagnostique in vitro professionnelle uniquement.
■ N'utilisez pas après la date d'expiration indiquée sur le package. N'utilisez pas le test si sa pochette en papier d'aluminium est endommagée. Ne réutilisez pas les tests.
■ Ce kit contient des produits d'origine animale. La connaissance certifiée de l'origine et / ou de l'état sanitaire des animaux ne garantit pas totalement l'absence d'agents pathogènes transmissibles. Il est donc recommandé que ces produits soient traités comme potentiellement infectieux et gérés par l'observation des précautions de sécurité habituelles (n'ingérez pas ou n'inhalez pas).
■ Évitez la contamination croisée des échantillons en utilisant un nouveau conteneur de collecte d'échantillons pour chaque échantillon obtenu.
■ Lisez attentivement l'intégralité de la procédure avant d'effectuer des tests.
■ Ne mangez pas, ne buvez pas, ne fumez pas dans la zone où les spécimens et les kits sont manipulés. Gérer tous les échantillons comme s'ils contenaient des agents infectieux. Observez les précautions établies contre les risques microbiologiques tout au long de la procédure et suivez les procédures standard pour l'élimination appropriée des échantillons. Portez des vêtements de protection tels que des manteaux de laboratoire, des gants jetables et une protection oculaire lorsque les échantillons sont testés.
■ N'échangez pas et n'échangez pas les réactifs de différents lots. Ne mélangez pas les bouchons de bouteilles de solution.
■ L'humidité et la température peuvent nuire aux résultats.
■ Lorsque la procédure de test est terminée, disposez soigneusement les écouvillons après les avoir automatiquement autoclacés à 121 ° C pendant au moins 20 minutes. Alternativement, ils peuvent être traités avec un hypochlorure de sodium à 0,5% (ou blanchi de maison) pendant une heure avant l'élimination. Les matériaux d'essai utilisés doivent être rejetés conformément aux réglementations locales, étatiques et / ou fédérales.
■ N'utilisez pas de pinceaux de cytologie avec des patients enceintes.
Stockage et stabilité
■ Le kit doit être stocké à 2-30 ° C jusqu'à imprimé la date d'expiration sur la pochet scellée.
■ Le test doit rester dans la pochette scellée jusqu'à l'utilisation.
■ Ne gèle pas.
■ Des soucis doivent être pris pour protéger les composants de ce kit contre la contamination. N'utilisez pas s'il existe des preuves de contamination microbienne ou de précipitations. La contamination biologique des équipements de distribution, des conteneurs ou des réactifs peut conduire à de faux résultats.
Collection et stockage spécialisés
■ Utilisez uniquement des écouvillons stériles à pointe de dacron ou de rayonne avec des arbres en plastique. Il est recommandé d'utiliser l'écouvillon fourni par le fabricant de kits (les écouvillons ne sont pas contenus dans ce kit, pour les informations de commande, veuillez contacter le fabricant ou le distributeur local, le numéro de catalcoge est 207000). Les écouvillons d'autres fournisseurs n'ont pas été validés. Les écouvillons avec des pointes de coton ou des arbres en bois ne sont pas recommandés.
■ Les sécrétions cervicovaginales sont obtenues à partir du fornix postérieur du vagin. Le processus de collecte est destiné à être doux. Une collection vigoureuse ou énergique, commune pour les cultures microbiologiques, n'est pas requise. Lors d'un examen du spéculum, avant tout examen ou manipulation du col ou du tractus vaginal, tournez légèrement la pointe de l'applicateur à travers le fornix postérieur du vagin pendant environ 10 secondes pour absorber les sécrétions cervicovaginales. Les tentatives ultérieures pour saturer la pointe de l'applicateur peuvent invalider le test. Retirez l'applicateur et effectuez le test comme indiqué ci-dessous.
■ Mettez l'écouvillon dans le tube d'extraction, si le test peut être exécuté immédiatement. Si les tests immédiats ne sont pas possibles, les échantillons de patients doivent être placés dans un tube de transport sec pour le stockage ou le transport. Les écouvillons peuvent être stockés pendant 24 heures à température ambiante (15-30 ° C) ou 1 semaine à 4 ° C ou pas plus de 6 mois à -20 ° C. Tous les échantillons doivent être autorisés à atteindre une température ambiante de 15-30 ° C avant les tests.
PROCÉDURE
Apportez des tests, des échantillons, du tampon et / ou des commandes à température ambiante (15-30 ° C) avant utilisation.
■ Placer un tube d'extraction propre dans la zone désignée du poste de travail. Ajouter 1 ml de tampon d'extraction dans le tube d'extraction.
■ Mettez l'écouvillon de l'échantillon dans le tube. Mélanger vigoureusement la solution en faisant tourner l'écouvillon avec force contre le côté du tube pendant au moins dix fois (tandis que submergé). Les meilleurs résultats sont obtenus lorsque l'échantillon est vigoureusement mélangé dans la solution.
■ Sortez autant de liquide que possible de l'écouvillon en pinçant le côté du tube d'extraction flexible lorsque l'écouvillon est retiré. Au moins 1/2 de la solution de tampon d'échantillon doit rester dans le tube pour une migration capillaire adéquate à se produire. Mettez le capuchon sur le tube extrait.
Jeter l'écouvillon dans un conteneur de déchets biohazard approprié.
■ Les échantillons extraits peuvent conserver à température ambiante pendant 60 minutes sans affecter le résultat du test.
■ Retirez le test de sa pochette scellée et placez-la sur une surface de niveau propre. Étiquetez l'appareil avec un patient ou un contrôle d'identification. Pour obtenir un meilleur résultat, le test doit être effectué dans un délai d'une heure.
■ Ajouter 3 gouttes (environ 100 µL) d'échantillon extrait du tube d'extraction au puits de l'échantillon sur la cassette d'essai.
Évitez de piéger les bulles d'air dans le (s) échantillon (s) et ne déposez aucune solution dans la fenêtre d'observation.
Alors que le test commence à fonctionner, vous verrez la couleur se déplacer à travers la membrane.
■ Attendez que le ou les groupes colorés apparaissent. Le résultat doit être lu à 5 minutes. N'interprétez pas le résultat après 5 minutes.
Jeter les tubes à essai utilisés et tester les cassettes dans un conteneur de déchets biohazard approprié.
Interprétation des résultats
| POSITIFRÉSULTAT:
| Deux bandes colorées apparaissent sur la membrane. Une bande apparaît dans la région de contrôle (C) et une autre bande apparaît dans la région de test (T). |
| NÉGATIFRÉSULTAT:
| Une seule bande colorée apparaît dans la région de contrôle (C). Aucune bande colorée apparente n'apparaît dans la région de test (T). |
| INVALIDERÉSULTAT:
| La bande de contrôle ne parvient pas à apparaître. Les résultats de tout test qui n'ont produit aucune bande de contrôle au temps de lecture spécifié doivent être rejetés. Veuillez consulter la procédure et répéter avec un nouveau test. Si le problème persiste, interrompez l'utilisation du kit immédiatement et contactez votre distributeur local. |
NOTE:
1. L'intensité de la couleur dans la région d'essai (t) peut varier en fonction de la concentration des substances visées présentes dans l'échantillon. Mais le niveau de substances ne peut pas être déterminé par ce test qualitatif.
2.
CONTRÔLE DE QUALITÉ
■ Les contrôles de procédure interne sont inclus dans le test. Une bande colorée apparaissant dans la région de contrôle (c) est considérée comme un contrôle procédural positif interne. Il confirme un volume d'échantillons suffisant et une technique procédurale correcte.
■ Les contrôles procéduraux externes peuvent être fournis (sur demande uniquement) dans les kits pour s'assurer que les tests fonctionnent correctement. De plus, les commandes peuvent être utilisées pour démontrer les performances appropriées par l'opérateur de test. Pour effectuer un test de contrôle positif ou négatif, complétez les étapes de la section de procédure de test traitant l'écouvillon témoin de la même manière qu'un échantillonnage d'échantillon.
Limitations du test
1. Ce test ne peut être utilisé que pour la détection qualitative de la fibronectine fœtale dans les sécrétions cervicovaginales.
2. Les résultats des tests doivent toujours être utilisés en conjonction avec d'autres données cliniques et de laboratoire pour la gestion des patients.
3. Les échantillons doivent être obtenus avant l'examen numérique ou la manipulation du col de l'utérus. Les manipulations du col de l'utérus peuvent conduire à des résultats faux positifs.
4. Les échantillons ne doivent pas être collectés si le patient a eu des rapports sexuels dans les 24 heures pour éliminer les résultats de faux positifs.
5. Les patients soupçonnés ou connues de la rupture placentaire, le placenta previa ou les saignements vaginaux modérés ou bruts ne doivent pas être testés.
6. Les patients atteints de cerclage ne doivent pas être testés.
7. Les caractéristiques de performance du fort®Le test FFN est basé sur des études sur des femmes avec des gestations de singleton. Les performances n'ont pas été vérifiées sur les patients avec des gestations multiples, par exemple, des jumeaux.
8. Le forttep®Le test FFN n'est pas destiné à être effectué en présence de rupture des membranes amniotiques et la rupture des membranes amniotiques doit être exclue avant de effectuer le test.
Caractéristiques de performance
Table
| Sensibilité relative: 97,96% (89,13% -99,95%) * Spécificité relative: 98,73% (95,50% -99,85%) * Accord global: 98,55% (95,82% -99,70%) * * Intervalle de confiance à 95% |
| Une autre marque |
| ||
| + | - | Total | |||
| Pas fort®fFn Test | + | 48 | 2 | 50 | |
| - | 1 | 156 | 157 | ||
|
| 49 | 158 | 207 | ||
Sensibilité analytique
La quantité détectable de FFN la plus faible dans l'échantillon extrait est de 50 μg / L.
Chez les femmes symptomatiques, des niveaux élevés (≥ 0,050 μg / ml) (1 x 10-7 mmol / L) de FFN entre 24 semaines, 0 jours et 34 semaines, 6 jours indiquent un risque accru de livraison en ≤ 7 ou ≤ 14 jours à compter de Collection d'échantillons. Parmi les femmes asymptomatiques, des niveaux élevés de FFN entre 22 semaines, 0 jours et 30 semaines, 6 jours indiquent un risque accru de livraison en ≤ 34 semaines, 6 jours de gestation. La coupure de 50 μg / L FFN a été établie dans une étude multicentrique menée pour évaluer l'association entre l'expression de la fibronectine fœtale pendant la grossesse et l'administration prématurée.
Substances interférentes
Il faut prendre soin de ne pas contaminer l'applicateur ou les sécrétions cervicovaginales avec des lubrifiants, des savons, des désinfectants ou des crèmes. Les lubrifiants ou les crèmes peuvent interférer physiquement avec l'absorption de l'échantillon sur l'applicateur. Les savons ou les désinfectants peuvent interférer avec la réaction anticorps-antigène.
Les substances interférentes potentielles ont été testées à des concentrations qui pourraient être raisonnablement trouvées dans les sécrétions cervicovaginales. Les substances suivantes n'ont pas interféré dans le test lorsqu'ils sont testés aux niveaux indiqués.
| Substance | Concentration | Substance | Concentration |
| Ampicilline | 1,47 mg / ml | Prostaglandine f2 | a0,033 mg / ml |
| Érythromycine | 0,272 mg / ml | Prostaglandine E2 | 0,033 mg / ml |
| Urine maternelle 3ème trimestre | 5% (vol) | Monistatr (miconazole) | 0,5 mg / ml |
| Pharmacie | 10 UI / ML | Carmin d'indigo | 0,232 mg / ml |
| Terbutaline | 3,59 mg / ml | Gentamicine | 0,849 mg / ml |
| Dexaméthasone | 2,50 mg / ml | Gel betadiner | 10 mg / ml |
| Mgso4•7h2o | 1,49 mg / ml | Nettoyant Betadiner | 10 mg / ml |
| Ritodrine | 0,33 mg / ml | K-YY Jelly | 62,5 mg / ml |
| Dermicidolr 2000 | 25,73 mg / ml |
Références de la littérature
1. Collège américain des obstétriciens et gynécologues. Travail prématuré. Bulletin technique, numéro 133, octobre 1989.
2. Creasy RK, Resnick R. Médecine maternelle et fœtale: principes et pratique. Philadelphie: WB Saunders; 1989.
3. Creasy RK, Merkatz IR. Prévention de la naissance prématurée: opinion clinique. Obstet Gynecol 1990; 76 (Suppl 1): 2S - 4S.
4. Morrison JC. Naissance prématurée: un puzzle à résoudre. Obstet Gynecol 1990; 76 (Suppl 1): 5S-12S.
5. Lockwood CJ, Senyei AE, Dische MR, Casal DC, et al. La fibronectine fœtale dans les sécrétions cervicales et vaginales comme prédicteur de l'accouchement prématuré. New Engl J Med 1991; 325: 669–74.
Glossaire des symboles
|
| Numéro de catalogue |  | Limitation de température |
 | Consulter des instructions pour une utilisation |
| Code par lots |
 | Dispositif médical diagnostique in vitro |  | Utiliser par |
 | Fabricant |  | Contient suffisamment |
 | Ne réutilisez pas |  | Représentant autorisé dans la communauté européenne |
 | CE marqué selon la directive IVD Medical Devices 98/79 / EC | ||
Liming Bio-Products Co., Ltd.
N ° 12 Huayuan Road, Nanjing, Jiangsu, 210042 PR China.
Tél: (0086) 25 85476723 Fax: (0086) 25 85476387
E-mail:sales@limingbio.com
Site Web: www.limingbio.com
www.stddiagnostics.com
www.stidiagnostics.com
Wellkang Ltd. (www.ce-marking.eu) Tél: +44 (20) 79934346
29 Harley St., London Wig 9qr, UK Fax: +44 (20) 76811874
Strongstep® Fetal Fibronectine Rapid Test Dispositif

La prestation prématurée, définie par l'American College of Obstetriciens and Gynecologists comme livraison avant la 37e semaine de gestation, est responsable de la majorité de la morbidité et de la mortalité périnatales non chromosomiques. Les symptômes de l'administration prématurée menacée comprennent les contractions utérines, le changement de débit vaginal, les saignements vaginaux, les maux de dos, l'inconfort abdominal, la pression pelvienne et les crampes. Les modalités de diagnostic pour l'identification de l'administration prématurée menacée comprennent la surveillance de l'activité utérine et les performances d'un examen cervical numérique, ce qui permet d'estimer les dimensions cervicales.
Le test rapide de la fibronectine fœtale Strongstep® est un test immunochromatographique visuellement interprété destiné à être utilisé pour la détection qualitative de la fibronectine fœtale dans les sécrétions cervicovaginales avec les caractéristiques suivantes:
Convivial:Procédure en une étape dans les tests qualitatifs
Rapide:Seulement 10 minutes requises pendant le même patient visitant
Sans équipement:Les hôpitaux limitant les sources ou le cadre clinique peuvent effectuer ce test
Livré:température ambiante (2 ℃ -30 ℃)