Un monde un combat
─ Coopération internationale pour construire une communauté mondiale de destin commun répondant au défi pandémique Covid-19
Le nouveau coronavirus qui balaye le monde a abouti à une crise pandémique mondiale de Covid-19. Le roman Coronavirus n'a pas de frontières, aucun pays ne sera épargné de cette bataille contre Covid-19. En réponse à cette pandémie mondiale Covid-19, Liming Bio-Product Corp apporte des contributions pour soutenir le bien-être de nos communautés mondiales.
Notre monde est actuellement confronté à l'impact sans précédent de la nouvelle pandémie de la maladie de Coronavirus 2019 (Covid-19). À ce jour, il n'y a pas de médicament efficace disponible pour le traitement de cette maladie. Cependant, de nombreux tests de diagnostic ont été développés pour la détection de Covid-19. Ces tests sont basés sur des méthodes moléculaires ou sérologiques pour détecter les nouveaux biomarqueurs d'acide nucléique ou d'anticorps spécifiques au coronavirus. Comme Covid-19 a atteint un statut pandémique, le diagnostic précoce de la nouvelle infection du coronavirus est essentiel pour évaluer la propagation du virus et la contenir, mais un test parfait pour une utilisation universelle n'existe pas encore. Nous devons savoir quels tests pourraient être utilisés pour le dépistage, le diagnostic et la surveillance de l'infection Covid-19, et quelles sont leurs limites. Il est très important de savoir à mieux utiliser ces outils scientifiques et à aider à identifier et à contrôler l'émergence de cette maladie grave rapide et grave.
Le but de la détection du nouveau coronavirus est de déterminer si un individu qui a une infection Covid-19 ou un porteur asymptotique qui peut répandre le virus en silence, pour fournir des informations essentielles pour guider la prise de décision pour le traitement clinique. Des études antérieures ont montré que 70% des décisions cliniques dépendent des résultats des tests. Lorsque différentes méthodes de détection sont utilisées, les exigences des kits de réactif de détection sont également différentes.
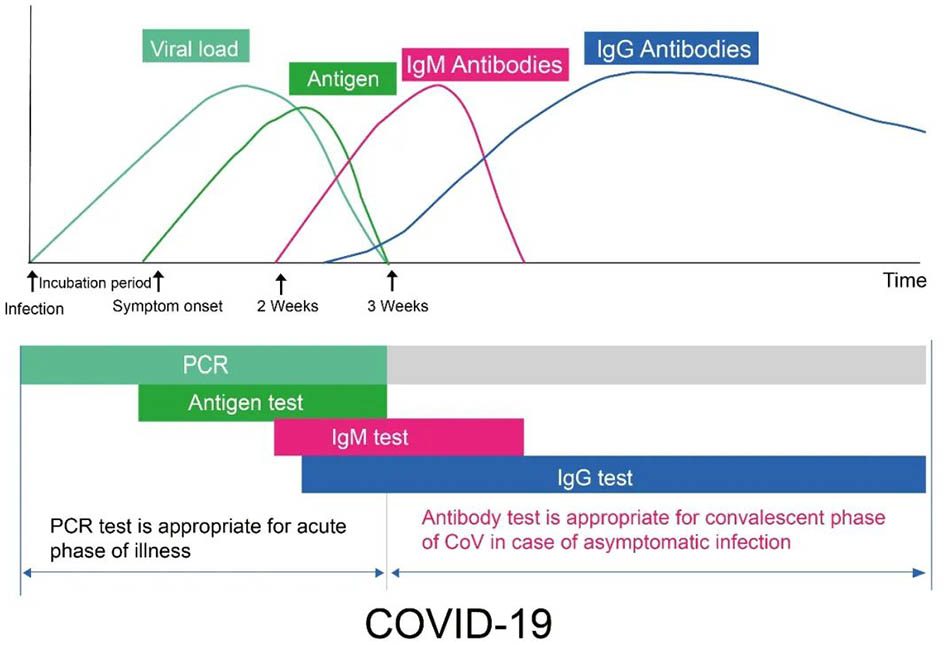
Figure 1
Figure1:Diagramme montrant les étapes clés des niveaux généraux de biomarqueurs au cours de l'évolution temporelle typique de l'infection Covid-19. L'axe des x indique le nombre de jours d'infection, et l'axe y indique la charge virale, la concentration d'antigènes et la concentration d'anticorps à différentes périodes. L'anticorps fait référence aux anticorps IgM et IgG. La détection de RT-PCR et d'antigène est utilisée pour détecter la présence ou l'absence de nouveau coronavirus, qui est une preuve directe de la détection précoce des patients. Dans la semaine suivant l'infection virale, la détection de PCR ou la détection d'antigène est préférée. Après la nouvelle infection au coronavirus pendant environ 7 jours, l'anticorps IgM contre le nouveau coronavirus a progressivement augmenté dans le sang du patient, mais la durée de l'existence est courte et sa concentration diminue rapidement. En revanche, l'anticorps IgG contre le virus apparaît plus tard, généralement environ 14 jours après l'infection par le virus. La concentration d'IgG augmente progressivement et persiste une longue période dans le sang. Ainsi, si l'IgM est détecté dans le sang du patient, cela signifie que le virus a récemment infecté, qui est un marqueur d'infection précoce. Lorsque l'anticorps IgG est détecté dans le sang du patient, cela signifie que l'infection virale est depuis un certain temps. Il est également appelé infection tardive ou infection précédente. On le voit souvent chez les patients en phase de récupération.
Les biomarqueurs du nouveau coronavirus
Le nouveau coronavirus est un virus d'ARN, qui est composé de protéines et d'acides nucléiques. Le virus envahit le corps hôte (humain), pénètre dans les cellules par le site de liaison correspondant au récepteur ACE2 et se réplique dans les cellules hôtes, ce qui fait répondre au système immunitaire humain aux envahisseurs étrangers et à produire des anticorps spécifiques. Par conséquent, les acides nucléiques du flacon et les antigènes et les anticorps spécifiques contre le nouveau coronavirus peuvent théoriquement être utilisés comme biomarqueurs spécifiques pour la détection du nouveau coronavirus. Pour la détection de l'acide nucléique, la technologie RT-PCR est la plus couramment utilisée, tandis que les méthodes sérologiques sont couramment utilisées pour la détection des nouveaux anticorps spécifiques au coronavirus. Actuellement, il existe une variété de méthodes de test disponibles que nous pouvons choisir pour tester l'infection Covid-19 [1].
Principes de base des principales méthodes d'essai pour le nouveau coronavirus
De nombreux tests de diagnostic pour CoVID_19 sont disponibles jusqu'à présent, avec plus de kits de test recevant une approbation sous une autorisation d'usage d'urgence chaque jour. Bien que les nouveaux développements de tests sortent de tant de noms et de formats différents, tous les tests actuels de Covid_19 reposent essentiellement sur deux technologies principales: la détection d'acide nucléique pour l'ARN viral et les immunoessais sérologiques qui détectent des anticorps viraux (IgM et IgG).
01. Détection d'acide nucléique
La réaction en chaîne de la transcription-polymérase inverse (RT-PCR), l'amplification isotherme médiée par la boucle (LAMP) et le séquençage de nouvelle génération (NGS) sont les méthodes d'acide nucléique communes pour la détection de nouveaux ARN de coronavirus. RT-PCR est le premier type de test pour Covid-19, recommandé à la fois par l'Organisation mondiale de la santé (OMS) et le Centre américain de contrôle et de prévention des maladies (CDC).
02. Détection des anticorps éréologiques
L'anticorps est une protéine protectrice produite dans le corps humain en réponse à l'infection virale. L'IGM est un type précoce d'anticorps tandis que l'IgG est un anticorps de type ultérieur. L'échantillon de sérum ou de plasma est généralement examiné pour la présence de types d'IgM et d'IgG spécifiques de l'anticorps pour l'évaluation des phases aiguës et de convalescence de l'infection Covid-19. Ces méthodes de détection basées sur des anticorps comprennent le test d'immunochromatographie en or colloïdal, l'immunochromatographie à l'immunochromatographie à la microsphère en latex ou à la microsphère fluorescente, le test d'immunosorbant lié à l'enzyme (ELISA) et le test de chimioluminescence.
03. Détection d'antigène viral
L'antigène est une structure sur le virus reconnu par le corps humain qui déclenche le système de défense immunitaire pour produire des anticorps pour nettoyer le virus du sang et des tissus. Un antigène viral présent sur le virus peut être ciblé et détecté en utilisant l'immunodosage. Comme l'ARN viral, les antigènes viraux sont également présents dans les voies respiratoires des individus infectés et peuvent être utilisés pour diagnostiquer la phase aiguë de l'infection Covid-19. Par conséquent, il est souvent recommandé de collecter des échantillons respiratoires supérieurs tels que la salive, les écouvillons nasopharyngés et oropharyngés, les dégustations de toux profonde, le liquide de lavage bronchoalvéolaire (BALF) pour les tests initiaux de l'antigène.
Sélection de méthodes de test pour le nouveau coronavirus
La sélection d'une méthode de test implique de nombreux facteurs, notamment le cadre clinique, les tests de contrôle de la qualité, le délai d'exécution, les coûts de test, les méthodes de collecte d'échantillonnage, les exigences techniques du personnel de laboratoire, les exigences de l'installation et de l'équipement. La détection des acides nucléiques ou des antigènes viraux est de fournir une preuve directe de la présence des virus et de confirmer le diagnostic d'une nouvelle infection au coronavirus. Bien qu'il existe de nombreuses méthodes de détection de l'antigène, leur sensibilité à la détection du nouveau coronavirus est théoriquement inférieure à celle de l'amplification RT-PCR. Le test d'anticorps est la détection d'anticorps antivirus produits dans le corps humain, qui est à la traîne dans le temps et ne peut souvent pas être utilisé pour une détection précoce pendant la phase aiguë de l'infection virale. Le cadre clinique pour les applications de détection peut varier et les sites de collecte d'échantillons peuvent également être différents. Pour la détection des acides nucléiques viraux et des antigènes, l'échantillon doit être collecté dans les voies respiratoires où le virus est présent, tels que les écouvillons nasopharyngés, les écouvillons oropharyngiens, les dégustations ou le liquide de lavage bronchoalvéolaire (BALF). Pour la détection basée sur des anticorps, l'échantillon sanguin doit être collecté et examiné pour la présence d'anticorps antivirus spécifiques (IgM / IgG). Cependant, les résultats des tests d'anticorps et d'acide nucléique peuvent se compléter mutuellement. Par exemple, lorsque le résultat des tests est l'acide nucléique négatif, IgM négatif mais IgG positif, ces résultats indiquent que le patient ne porte pas actuellement le virus, mais a été récupéré de la nouvelle infection du coronavirus. [2]
Avantages et inconvénients des nouveaux tests de coronavirus
Dans le protocole de diagnostic et de traitement pour une nouvelle pneumonie du coronavirus (version d'essai7) (publié par la Commission nationale de la santé et l'administration de la médecine chinoise traditionnelle le 3 mars 2020), les tests d'acide nucléique sont utilisés comme méthode de la norme pour le diagnostic du roman Infection par le coronavirus, tandis que les tests d'anticorps sont également considérés comme l'une des méthodes de confirmation du diagnostic.

Résultats pathogènes et sérologiques
(1) Résultats pathogènes: un nouvel acide nucléique de coronavirus peut être détecté dans les écouvillons nasopharyngés, les expectorations, les sécrétions de voies respiratoires inférieures, le sang, les excréments et d'autres échantillons en utilisant des méthodes RT-pcrand / ou NGS. Il est plus précis si les échantillons sont obtenus à partir des voies respiratoires inférieures (extraction des expectorations ou des voies d'air). Les spécimens doivent être soumis pour les tests dès que possible après la collecte.
(2) Résultats sérologiques: IgM spécifique au virus NCP devient détectable environ 3 à 5 jours après le début; L'IgG atteint un titrage d'au moins 4 fois augmenter pendant la convalescence par rapport à la phase aiguë.
Cependant, la sélection des méthodes de test dépend des emplacements géographiques, des réglementations médicales et des milieux cliniques. Aux États-Unis, le NIH a publié des directives de traitement de la maladie de Coronavirus 2019 (Covid-19) (site mises à jour: 21 avril 2010) et la politique de la FDA pour les tests de diagnostic pour la maladie du coronavirus-2019 pendant l'urgence de la santé publique (publiée le 16 mars 20102020 ), dans lequel les tests sérologiques des anticorps IgM / IgG sélectionnés uniquement comme test de dépistage.
Méthode de détection d'acide nucléique
RT_PCR est un test d'acide nucléique très sensible conçu pour détecter si le nouvel ARN du coronavirus est présent ou non dans le spécimen respiratoire ou autre. Un résultat de test de PCR positif signifie la présence d'un nouvel ARN de coronavirus dans l'échantillon pour confirmer l'infection Covid-19. Un résultat de test de PCR négatif ne signifie pas l'absence de l'infection par le virus car elle pourrait être affectée par une mauvaise qualité de l'échantillon ou un moment de la maladie à la phase récupérée, etc. Bien que RT-PCR soit un test très sensible, il présente plusieurs inconvénients. Les tests RT-PCR peuvent être à forte intensité de main-d'œuvre et longs, en fonction de la haute qualité de l'échantillon. Cela peut être un défi car la quantité d'ARN viral varie non seulement considérablement entre les différents patients, mais peut également varier au sein du même patient en fonction des points de temps où l'échantillon est prélevé ainsi que des phases d'infection ou l'apparition des symptômes cliniques. La détection du nouveau coronavirus nécessite des spécimens de haute qualité qui contiennent une quantité suffisante d'ARN viral intact.
Le test RT-PCR peut donner un résultat négatif incorrect (faux négatif) pour certains patients qui ont une infection Covid-19. Comme nous le savons, les principaux sites d'infection du nouveau coronavirus sont situés dans le poumon et les voies respiratoires inférieures, comme les alvéoles et les bronches. Par conséquent, l'échantillon d'expectorations d'une toux profonde ou du liquide de lavage bronchoalvéolaire (BALF) considéré comme ayant la sensibilité la plus élevée pour la détection virale. Cependant, dans la pratique clinique, les échantillons sont souvent prélevés dans les voies respiratoires supérieures en utilisant des écouvillons nasopharyngés ou oropharyngés. La collecte de ces spécimens est non seulement inconfortable pour les patients, mais nécessite également du personnel spécialement formé. Pour rendre l'échantillonnage moins invasif ou plus facile, dans certains cas, les patients peuvent recevoir un écouvillonnage oral et leur permettre de prélever un échantillon de la muqueuse buccale ou de la langue s'écouler. Sans ARN viral suffisant, RT-QPCR peut renvoyer un résultat de test faux négatif. Dans la province de Hubei, en Chine, la sensibilité à la RT-PCR dans la détection initiale n'a été signalée qu'environ 30% à 50%, avec une moyenne de 40%. Le taux élevé de faux négatifs a probablement été causé par un échantillonnage insuffisant.
De plus, le test RT-PCR nécessite du personnel hautement formé pour effectuer des étapes d'extraction d'ARN complexes et une procédure d'amplification par PCR. Il nécessite également un niveau plus élevé de protection de biosécurité, une installation de laboratoire spéciale et un instrument de PCR en temps réel. En Chine, le test RT-PCR pour la détection de Covid-19 doit être effectué dans les laboratoires de niveau de biosécurité 2 (BSL-2), la protection du personnel utilisant la pratique de niveau de biosécurité 3 (BSL-3). En vertu de ces exigences, du début de janvier à début février 2020, la capacité du laboratoire CDC de Chine Wuhan n'a pu détecter que quelques centaines de cas par jour. Normalement, ce ne serait pas un problème lors du test d'autres maladies infectieuses. Cependant, lorsqu'il s'agit d'une pandémie mondiale telle que Covid-19 avec des millions de personnes potentiellement testées, la RT-PCR devient un problème critique en raison de ses exigences pour des installations de laboratoire spéciales ou des équipements techniques. Ces inconvénients peuvent limiter le RT-PCR à être utilisé comme un outil efficace pour le dépistage, et peuvent également entraîner des retards dans les rapports des résultats des tests.
Méthode de détection d'anticorps sérologiques
Avec les progrès de l'évolution de la maladie, en particulier aux stades moyen et tardifs, le taux de détection des anticorps est très élevé. Une étude à l'hôpital Wuhan Central South a montré que le taux de détection des anticorps pouvait atteindre plus de 90% au cours de la troisième semaine d'infection Covid-19. De plus, l'anticorps est le produit de la réponse immunitaire humaine contre le nouveau coronavirus. Le test d'anticorps offre plusieurs avantages par rapport à la RT-PCR. Premièrement, l'anticorps sérologique teste simple et rapide. Les tests d'écoulement latéral des anticorps peuvent être utilisés pour le point de service afin de livrer un résultat en 15 minutes. Deuxièmement, la cible détectée par le test sérologique est l'anticorps, qui est connu pour être beaucoup plus stable que l'ARN viral. Pendant la collecte, le transport, le stockage et les tests, les échantillons pour les tests d'anticorps sont généralement plus stables que les échantillons pour RT-PCR. Troisièmement, comme l'anticorps est réparti uniformément dans la circulation sanguine, il y a moins de variation d'échantillonnage par rapport au test d'acide nucléique. Le volume d'échantillon requis pour le test des anticorps est relativement faible. Par exemple, 10 microliter de sang de piqûre de doigt sont suffisants pour être utilisés dans le test d'écoulement latéral de l'anticorps.
En général, le test d'anticorps est choisi comme outil de supplément pour la détection de l'acide nucléique afin d'améliorer le taux de détection du nouveau coronavirus pendant les cours de maladie. Lorsque le test des anticorps est utilisé avec un test d'acide nucléique, il peut augmenter la précision du test pour le diagnostic de Covid19 en réduisant les résultats potentiels en fausse positif et faussement négatif. Le guide de fonctionnement actuel ne recommande pas d'utiliser deux types de test séparément comme format de détection indépendant, mais doit être utilisé comme format combiné. [2]
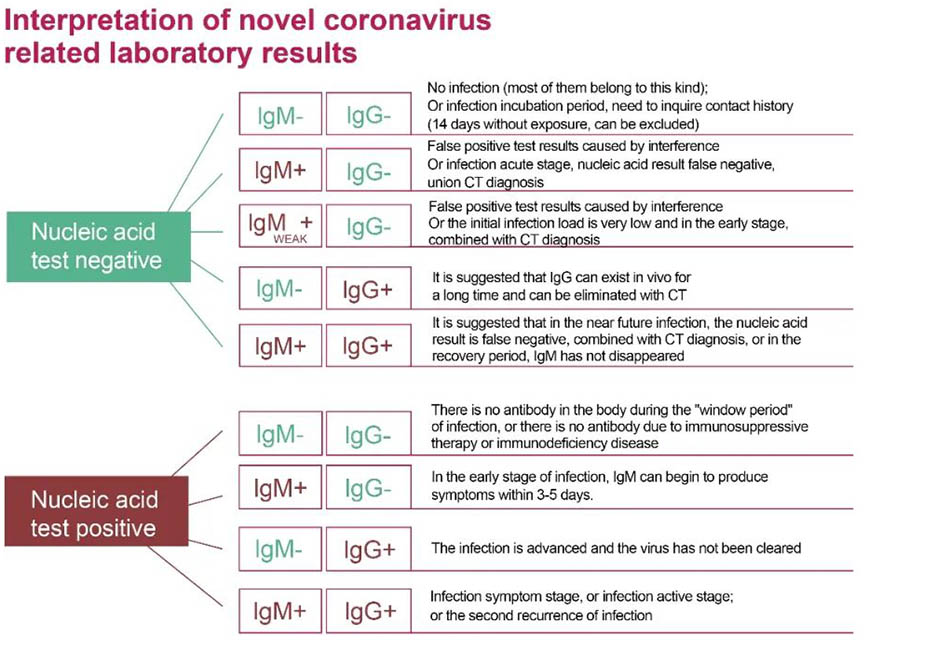
Figure2:L'interprétation correcte des résultats des tests d'acide nucléique et d'anticorps pour la détection d'une nouvelle infection au coronavirus

Figure 3:Liming Bio-Products Co., Ltd. - New Coronavirus IgM / IgG Antibody Dual Rapid Test Kit (Strongstep®Test rapide de l'anticorps IgM / IgG SARS-COV-2, immunochromatographie en latex)

Figure 4:Liming Bio-Products Co., Ltd. - Strongstep®Nouvel kit de PCR en temps réel du coronavirus (SARS-COV-2) (détection pour trois gènes, méthode de la sonde fluorescente).
Note:Ce kit de PCR très sensible et prêt à l'emploi est disponible en format lyophilisé (processus de séchage auge) pour un stockage à long terme. Le kit peut être transporté et stocké à température ambiante et est stable pendant un an. Chaque tube de prémélange contient tous les réactifs nécessaires à l'amplification par PCR, y compris la transcriptase inverse, la polymérase Taq, les amorces, les sondes et les substrats DNTPS. sur un instrument PCR pour exécuter l'amplification.
En réponse à la nouvelle épidémie de coronavirus, Liming Bio-Products Co., Ltd. a travaillé rapidement pour développer deux kits de diagnostic pour permettre aux laboratoires de santé clinique et publique de diagnostiquer rapidement l'infection à Covid-19. Ces kits sont très adaptés à une utilisation pour le dépistage à grande échelle dans les pays et les régions où la nouvelle épidémie de coronavirus se propage rapidement et pour assurer le diagnostic et la confirmation de l'infection Covid-19. Ces kits sont utilisés uniquement sous l'autorisation d'utilisation d'urgence pré-notifiée (PEUA). Les tests sont limités aux laboratoires certifiés en vertu des réglementations des autorités nationales ou locales.
Méthode de détection de l'antigène
1. La détection de l'antigène viral est classée dans la même catégorie de détection directe que la détection de l'acide nucléique. Ces méthodes de détection directe recherchent des preuves d'agents pathogènes viraux dans l'échantillon et peuvent être utilisés pour le diagnostic de confirmation. Cependant, le développement de kits de détection d'antigène nécessite une haute qualité d'anticorps monoclonaux avec une forte affinité et une sensibilité élevée capable de reconnaître et de capturer des virus pathogènes. Il faut généralement plus de six mois pour sélectionner et optimiser un anticorps monoclonal adapté à une utilisation dans la préparation du kit de détection de l'antigène.
2. Actuellement, les réactifs pour la détection directe du nouveau coronavirus sont toujours en phase de recherche et de développement. Par conséquent, aucun kit de détection d'antigène n'a été cliniquement validé et disponible dans le commerce. Bien qu'il ait déjà été signalé qu'une entreprise de diagnostic à Shenzhen a développé un kit de détection d'antigène et testé cliniquement en Espagne, la fiabilité et la précision du test n'ont pas pu être validées en raison de la présence de problèmes de qualité des réactifs. À ce jour, la NMPA (ancienne FDA China) n'a encore approuvé aucun kit de détection d'antigène pour une utilisation clinique. En conclusion, une variété de méthodes de détection ont été développées. Chaque méthode présente ses avantages et ses limites. Les résultats de différentes méthodes peuvent être utilisés pour la vérification et le complément.
3. Produire un kit de test Covid-19 de qualité dépend fortement de l'optimisation pendant la recherche et le développement. Liming Bio-Product Co., Ltd. Des kits de test sont nécessaires pour répondre aux normes strictes de fabrication et de contrôle de la qualité pour s'assurer qu'elles fournissent les niveaux les plus élevés de performances et de cohérence. Les scientifiques de Liming Bio-Product Co., Ltd. ont plus de vingt ans d'expérience dans la conception, les tests et l'optimisation des kits de diagnostic in vitro pour assurer le plus haut niveau de performance dans la quantification analytique.
Pendant la pandémie Covid-19, le gouvernement chinois a été confronté à l'énorme demande de matériel de prévention épidémique dans les points chauds internationaux. Le 5 avril, lors de la conférence de presse du mécanisme de prévention et de contrôle conjoint du Conseil d'État "renforçant la gestion de la qualité des matériaux médicaux et réglementant l'ordre du marché", Jiang Fan, un inspecteur de premier niveau du Département du commerce extérieur du ministère du ministère du commerce, a déclaré: "Ensuite, nous concentrerons nos efforts sur deux aspects, d'abord, pour accélérer le soutien de plus de fournitures médicales nécessaires à la communauté internationale, et également, pour améliorer le contrôle de la qualité, la réglementation et la gestion des produits. Nous apporterons la contribution de la Chine à répondre conjointement à l'épidémie mondiale et à bâtir une communauté avec un avenir commun pour l'humanité.



Figure 5:Le nouveau réactif de Coronavirus de Liming Bio-Products Co., Ltd.
Le certificat honoraire


Houshenshan
Figure 6. Liming Bio-Product Co., Ltd. a soutenu l'hôpital de montagne Wuhan Vulcan (Houshenshan) pour lutter contre l'épidémie Covid-19 et a reçu le certificat honoraire de la Croix-Rouge de Wuhan. L'hôpital Wuhan Vulcan Mountain est l'hôpital le plus célèbre de Chine qui se spécialise dans le traitement des patients grave - 19 patients.
Alors que la nouvelle épidémie de coronavirus continue de se propager dans le monde entier, Nanjing Liming Bio-Product Co., Ltd. intensifie pour soutenir et aider les communautés dans le monde entier avec nos technologies innovantes pour lutter contre cette menace mondiale sans précédent. Les tests rapides de l'infection Covid-19 sont un élément essentiel de la lutte contre cette menace. Nous continuons de contribuer de manière significative en fournissant des plates-formes de diagnostic de haute qualité entre les mains des travailleurs de la santé de première ligne afin que les gens puissent recevoir les résultats critiques des tests dont ils ont besoin. Les efforts de Liming Bio-Produit Co., Ltd. dans la bataille contre la pandémie Covid-19 sont de contribuer à nos technologies, nos expériences et notre expertise aux communautés internationales pour la construction d'une communauté mondiale de destin.
Appuyez sur longue ~ scan et suivez-nous
E-mail: sales@limingbio.com
Site Web: https://limingbio.com
Heure du poste: mai-01-2020







