Dispositif système Strongstep pour le test rapide de l'antigène SARS-COV-2
Utilisation prévue
Le dispositif du système StrongStep® pour l'antigène SARS-COV-2 Test Rapid utilise une technologie d'immunochromatographie pour détecter l'antigène nucléocapside SARS-COV-2 dans la salive humaine. Ce test est uniquement utilisé et destiné aux tests SEI. Il est recommandé d'utiliser ce test dans les 7 jours suivant l'apparition des symptômes. Il est étayé par l'évaluation des performances cliniques.
INTRODUCTION
Les nouveaux coronavirus appartiennent au genre 0. Covid-19 est une maladie infectieuse respiratoire aiguë. Les gens sont généralement sensibles. Actuellement, les patients infectés par le nouveau coronavirus sont la principale source d'infection basée sur l'étude épidémiologique actuelle, la période d'incubation est de 1 à 14 jours, principalement de 3 à 7 jours. Les principales manifestations comprennent la fièvre, la fatigue et la toux sèche. La congestion nasale, le nez qui coule, le mal de gorge, la myalgie et la diarrhée se trouvent dans quelques cas.
PRINCIPE
Le dispositif du système StrongStep® pour le test d'antigène SARS-COV-2 utilise un test immunochromatographique, ce kit recueille des échantillons de salive à partir du bâton d'adsorption de salive à l'avant de la carte de test, et les échantillons de salive avancent dans l'action capillaire. Si l'échantillon contient un antigène de protéine SARS-COV-2 N.Il est identifié et lié par des anticorps marqués sur la surface du latex pour former un complexe immunitaire. Lorsque le complexe immunitaire formé migre vers la ligne de détection de la membrane des fibres d'acide nitrique, pour identifier les anticorps emballés et former une ligne de détection fuchsia (T-Lins), montrant l'antigène SARS-CoV-2 positif; Si la ligne T ne montre pas de couleur, c'est un résultat négatif. Une autre ligne sur la membrane en fibre d'acide nitrique est remplie d'anticorps de streptavidine comme ligne de contrôle de la qualité (ligne C), pour indiquer un processus de test efficace.
PRÉCAUTIONS
• Ce kit est pour une utilisation diagnostique in vitro uniquement.
• Ce kit peut être administré par du personnel médical ou non médical en suivant les instructions de fonctionnement.
• Lisez attentivement les instructions avant d'effectuer le test.
• Ce produit ne contient aucun matériau source humain.
• N'utilisez pas le contenu du kit après la date d'expiration.
• Gérez tous les spécimens comme potentiellement infectieux.
• Ne pas réactif de pipette par la bouche et sans fumer ou manger lors des tests.
• Portez des gants pendant toute la procédure.
Stockage et stabilité
Les sachets scellés du kit de test peuvent être stockés entre 2 et 30 ° C pendant la durée de la durée de conservation comme indiqué sur la poche.
Collection et stockage des spécimens
Le meilleur spécimen de salive devrait être collecté le matin après juste le réveil. Ne mangez ni ne buvez rien pendant 30 minutes avant de récupérer votre échantillon de salive. Faites-le avant de prendre un café, de prendre le petit déjeuner ou de vous brosser les dents - ou d'attendre que vous n'ayez rien consommé dans les 30 minutes précédentes.
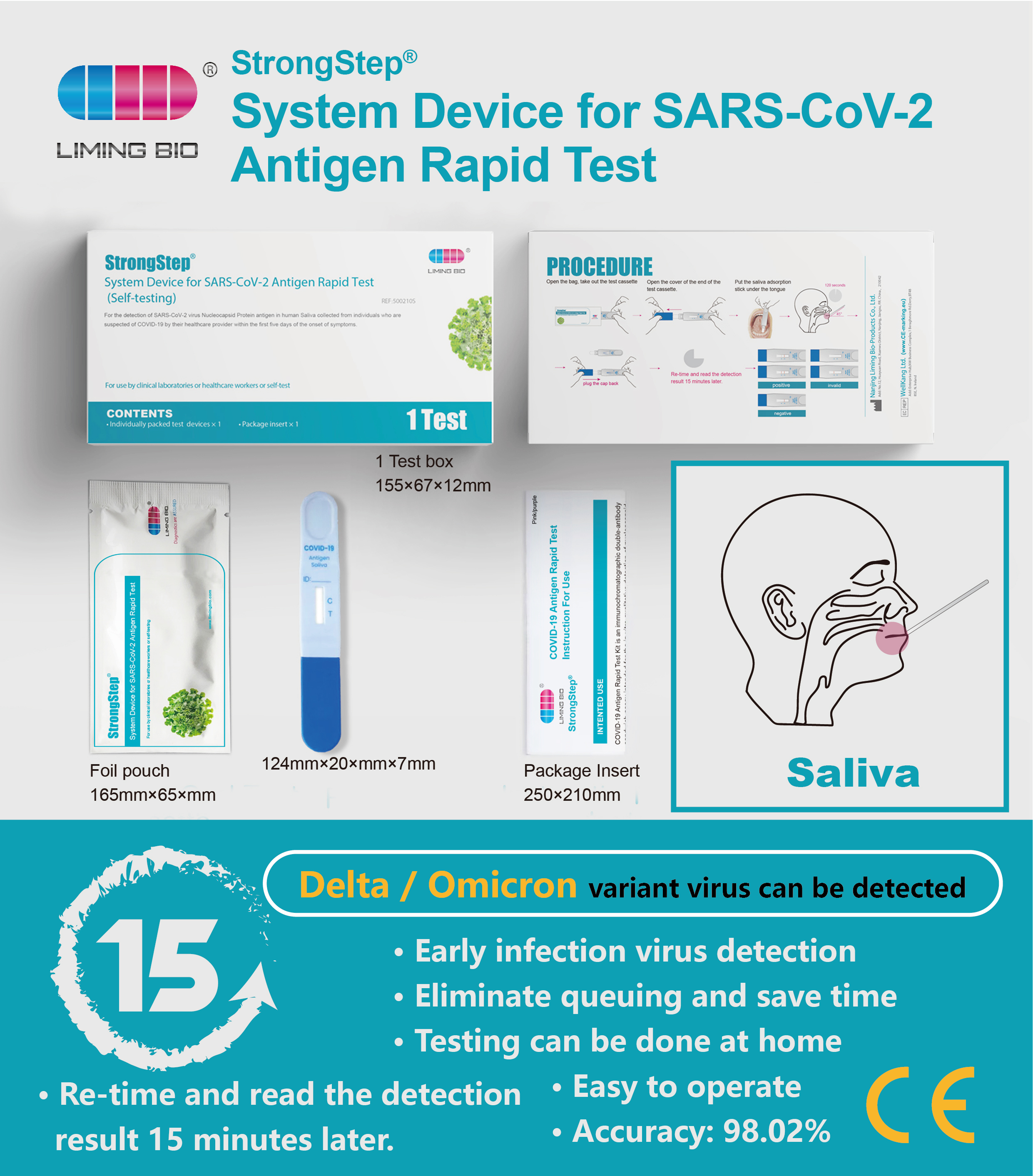
PROCÉDURE
Apporter des tests à température ambiante (15-30 ° C) avant utilisation.
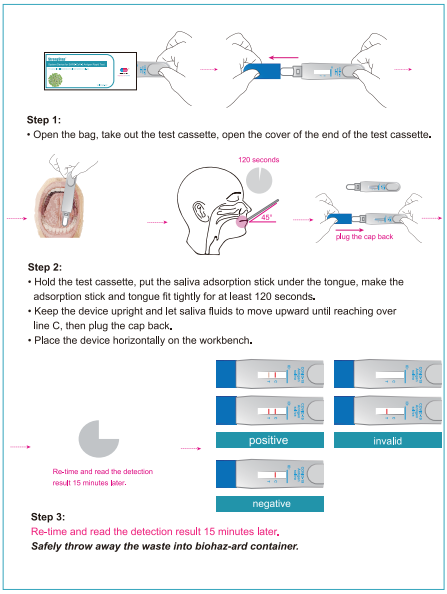
Étape 1:
Ouvrez le sac, retirez le dispositif de test, ouvrez la couverture de l'extrémité du dispositif de test.
Étape 2:
• Tenez la cassette de peur, mettez le bâton d'adsorption de salive sous la langue, faites bien s'adapter le bâton d'adsorption pendant au moins 120 secondes.
• Gardez l'appareil debout et laissez les fluides de salive se déplacer vers le haut jusqu'à atteindre la ligne C, puis brancher le capuchon.
• Placez le périphérique horizontalement sur l'ouchette.
Étape 3:
Re-temps et lisez la détection Resuh 15 minutes plus tard.
Jetez en toute sécurité les déchets dans un récipient biohaz-ter.
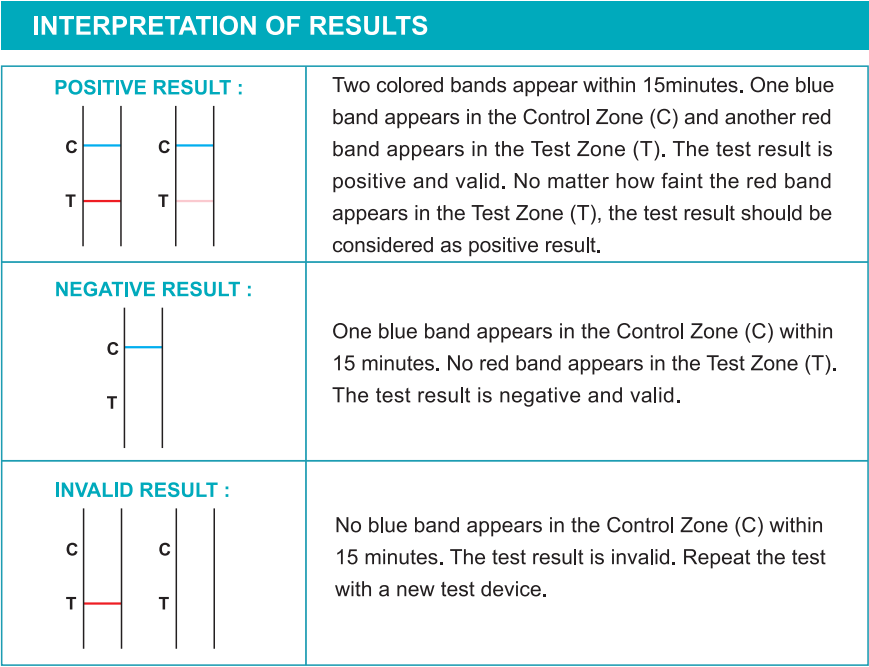
CONTRÔLE DE QUALITÉ
Les contrôles de procédure interne sont inclus dans le test. Une bande bleue apparaissant dans la région de contrôle (c) est considérée comme un contrôle procédural interne. Il confirme un volume d'échantillons suffisant et une technique procédurale correcte.
Limitations du test
1. Le kit est destiné à utiliser pour la détection qualitative des antigènes SAR-COV-2 de la salive.
2. Ce test détecte à la fois SARS viable (en direct) et non viable. Les performances du test dépendent de la quantité de virus (antigène) dans l'échantillon et peuvent ou non être en corrélation avec les résultats de la culture virale effectués sur le même échantillon.
3. Un résultat de test négatif peut se produire si le niveau d'antigène dans un échantillon est inférieur à la limite de détection du test ou si l'échantillon a été collecté ou transporté de manière incorrecte.
4. Le non-respect de la procédure de test peut nuire aux performances du test et / ou invalider le résultat du test.
5. Le kit est pour un dépistage présumé uniquement. Les résultats négatifs n'excluent pas l'infection SARS-COV-2 et la personne n'étant pas infectieuse. Si des symptômes sont présents, recherchez immédiatement des tests supplémentaires.
6. Les résultats des tests doivent être corrélés avec les antécédents cliniques, les données épidémiologiques et d'autres données disponibles pour le clinicien évaluant le patient.
7. Les résultats positifs des tests n'excluent pas les co-infections avec d'autres agents pathogènes et ne peuvent pas nécessairement déterminer si une personne est infectieuse.
8. Les résultats des tests négatifs ne sont pas destinés à régner dans d'autres infections virales ou bactériennes non-SARS.
9. Les résultats négatifs des patients présentant des symptômes doivent être traités comme présumés et confirmés par un test moléculaire autorisé de la FDA local, si nécessaire, pour la gestion clinique, y compris le contrôle des infections.
10. Les recommandations de stabilité des échantillons sont basées sur les données de stabilité des tests de grippe et les performances peuvent être différentes avec le SRAS-COV-2. Les utilisateurs doivent tester les spécimens le plus rapidement possible après la collecte des échantillons.
11. plus bas en raison de sa méthodologie.
12. Les valeurs prédictives positives et négatives dépendent fortement des taux de prévalence.
Les résultats des tests positifs sont plus susceptibles de représenter les résultats de faux positifs pendant les périodes d'activité peu / pas de SAR-COV-2 lorsque la prévalence de la maladie est faible. Les résultats des tests négatifs de la maladie sont plus susceptibles lorsque la prévalence de la maladie causée par le SRAS-COV-2 est élevée.
13. Les anticorps monoclonaux peuvent ne pas détecter ou détecter avec moins de sensibilité, les virus de la grippe SARS-COV-2 qui ont subi des changements d'acides aminés mineurs dans la région d'épitope cible.
14. Les performances de ce test n'ont pas été évaluées pour une utilisation chez les patients sans signes et symptômes d'infection respiratoire et de performance peuvent différer chez les individus asymptomatiques.
15. La quantité d'antigène dans un échantillon peut diminuer à mesure que la durée de la maladie augmente.
Les échantillons prélevés après le jour 7 de la maladie sont plus susceptibles d'être négatifs par rapport à un test RT-PCR.
La sensibilité du test après les sept jours de début des symptômes a été connue pour diminuer par rapport à un test RT-PCR.
16. Il n'est pas recommandé d'utiliser des spécimens de supports de transport de virus (VTM) dans ce test, si les clients insistent pour utiliser ce type d'échantillon, les clients doivent se valider.
17. Des tests fréquents sont nécessaires pour augmenter la sensibilité du diagnostic de Covid-19.
18. Aucune baisse de sensibilité par rapport au type sauvage par rapport aux variantes suivantes -B.1.1.7; B.1.351; B.1.2; B.1.1.28; B.1.617; B.1.1.529.
19. Les résultats positifs indiquent que les antigènes viraux ont été détectés dans l'échantillon prélevé, veuillez vous auto-qualifier et informer rapidement votre médecin de famille et / ou votre service de santé local conformément aux exigences de l'État.
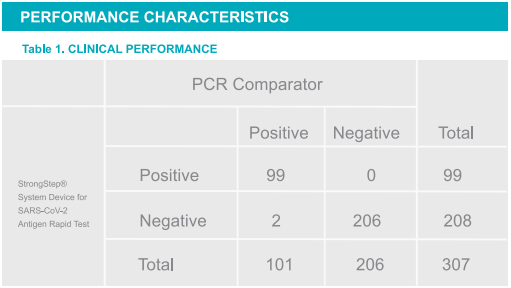
Pourcentage positif Accord: (PPA) = 98,02% (93,03% ~ 99,76%) *
Pourcentage négatif Accord: (NPA) = 100% (98,23% ~ 100%) *
Taux de coïncidence total = 98,76%
* Intervalle de confiance à 95%
Performance analytique
a) Limite de détection (LOD):
La limite de détection (LOD) du test a été déterminée en utilisant des dilutions limitantes des SARS-CoV-2 inactivés. Il s'agit d'une préparation du coronavirus-2 lié au SRAS (SARS-COV-2), isolant dans le CDC chinois, qui a été inactivé par la β-propopone. Le matériau a été fourni congelé à une concentration de TCID50de 5,00 x105/ ml.
Pour déterminer le SARS-COV-2 pour refléter le test lors de l'utilisation de la salive directe. Dans cette étude, environ 50 μl de la dilution du virus ont été enrichies avec l'échantillon de salive négatif.
Le LOD a été déterminé en trois étapes:
1. Dépistage de LOD
Des dilutions de 10 fois du virus inactivé ont été faites dans une salive négative et traitées pour chaque étude comme décrit ci-dessus. Ces dilutions ont été testées en triple. La concentration démontrant 3 des 3 positifs a été choisie pour la recherche de l'aire de répartition.
2. Recherche de gamme de lod
Cinq (5) des dilutions de doublement ont été faites du TCID50de 5,00 x102/ Concentration ML dans la salive négative traitée pour l'étude comme décrit ci-dessus. Ces dilutions ont été testées en triple. La concentration démontrant 3 des 3 positifs a été choisie pour la confirmation du LOD.
3. Confirmation de LOD
La concentration tcid50de 2,50 x102/ La dilution ML a été testée pour un total de vingt (20) résultats. Au moins dix-neuf (19) des vingt (20) résultats étaient positifs.
Conclusion:
Sur la base de ces tests, la concentration a été confirmée comme suit:
LOD: TCID502,50 x102/ ml
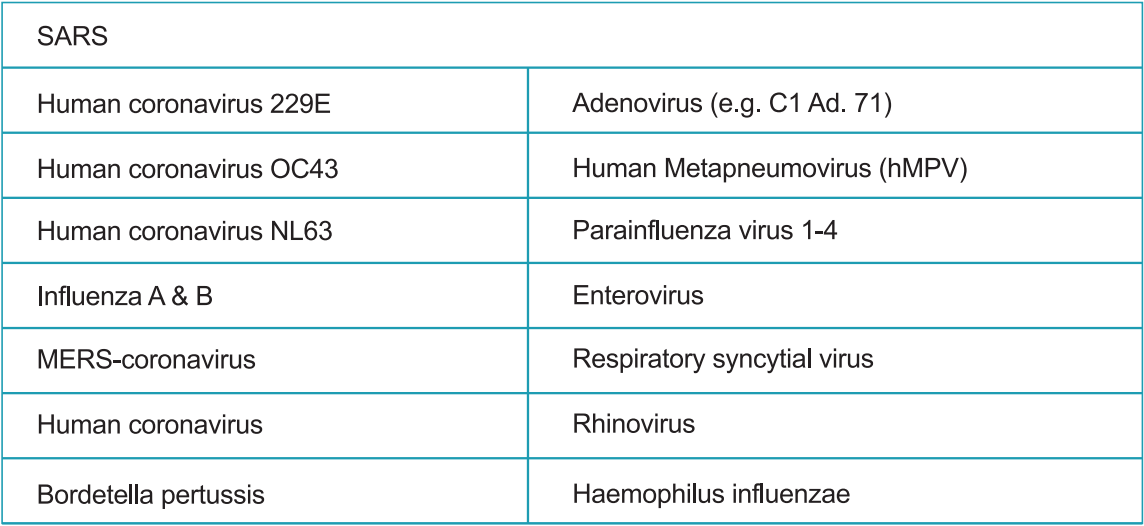
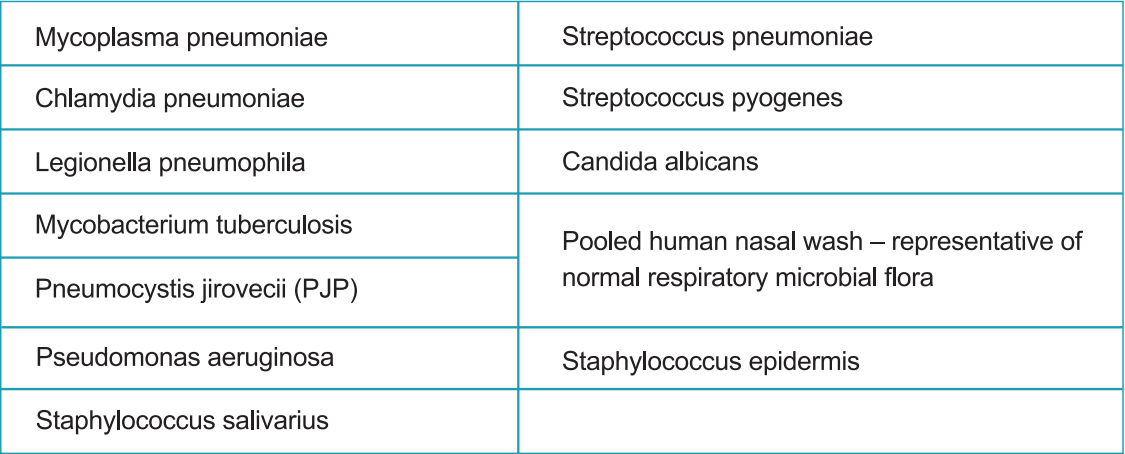
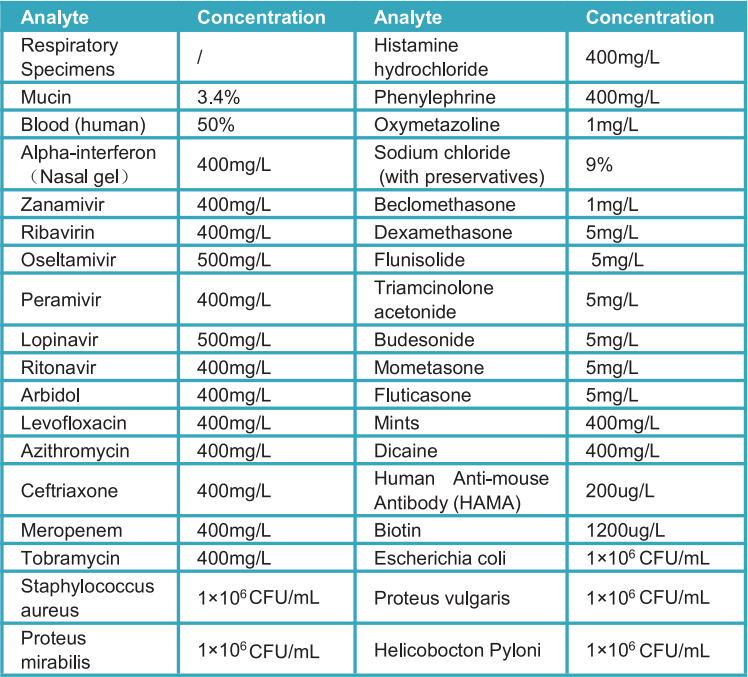
b) Réactivité croisée:
La réactivité croisée du test rapide de l'antigène SARS-CoV-CoV-2 du système StrongStep® a été évaluée en testant divers micro-organismes (10⁶ CFU / ml), des virus (10⁵ PFU / ml) et des matrices négatives qui peuvent potentiellement réactiver avec le Strongstep® Test rapide de l'antigène SARS-COV-COV-2.
Chaque organisme et virus a été testé en triple. Sur la base des données générées par cette étude, le dispositif du système StrongStep® pour le test rapide de l'antigène SARS-COV-2 ne réagit pas avec les organismes ou les virus testés.
c) Interférer la substance:
Les substances interférentes potentielles du test rapide de l'antigène SROSSTEP® SARS-COV-2 ont été évaluées en testant diverses substances avec une concentration ci-dessous qui peuvent potentiellement interférer avec le test rapide de l'antigène SRAS-CoV-2 StrongStep®. Chaque substance a été testée en triple. Sur la base des données générées par cette étude, le test rapide de l'antigène SROSSTEP® SARS-COV-2 n'interfère pas avec les substances testées.
d) Effet de crochet
La concentration la plus élevée de stock SARS-CoV-2 inactivé par la chaleur disponible (TCID50de 5,00 x 105/ ml) a été testé. Aucun effet de crochet n'a été détecté.




1人份抗原卡实物图唾液版1_00_副本-300x216.png)